Por Dra. Ana Magalhães, Investigadora de Cancro da Mama Metastático, no Advanced Breast Cancer Translational Laboratory, do Instituto Gulbenkian de Medicina Molecular.
A maioria das mortes associadas ao Cancro da Mama ocorre devido à formação de metástases, ou seja, quando células tumorais se espalham para outros órgãos que não a mama, como pulmões, fígado, ossos ou cérebro.
Os números mostram bem o impacto:
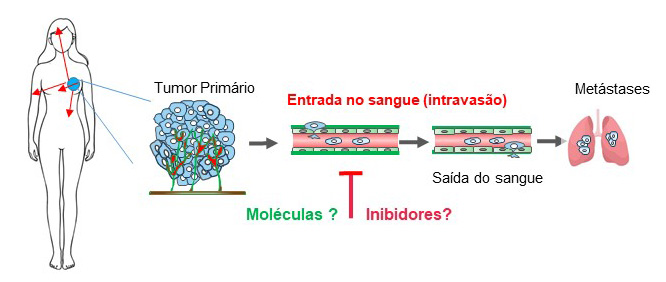
Sabe-se que a principal via pela qual as células de Cancro da Mama chegam a outros órgãos é a corrente sanguínea (2). Assim, em teoria, se conseguirmos impedir a entrada de células de Cancro da Mama nessa circulação – processo chamado intravasão – poderemos prevenir a formação de metástases e salvar vidas (um dos principais focos da minha investigação).
No âmbito da parceria entre a CA Vida e a Fundação GIMM, acompanhamos agora os avanços alcançados por mim e por uma estudante de mestrado orientada por mim no Advanced Breast Cancer Translational Laboratory. O nosso objetivo é estudar precisamente os mecanismos moleculares que regulam a intravasão, um passo importante para travar a metastização.
Neste sentido, nos últimos anos, desenvolvemos um sistema inovador de co-cultura de células de Cancro da Mama e células de vasos sanguíneos (endoteliais), permitindo recriar em laboratório o processo de intravasão.
Mais recentemente, criámos, utilizando este modelo, um ensaio capaz de quantificar o número de células tumorais que atravessam a parede dos vasos sanguíneos em 24 horas.
Graças a este ensaio, demonstrámos que um fármaco inibidor da mobilidade celular consegue reduzir significativamente a intravasão. Este resultado confirma a robustez da plataforma que pode ser usada para:
Atualmente, estamos a avaliar se o mesmo sistema pode ser usado para testar simultaneamente a eficácia dos potenciais fármacos no bloqueio da intravasão e a eventual toxicidade nos vasos sanguíneos.
Se for validado, este avanço aumentará consideravelmente a relevância da plataforma, permitindo avaliar em paralelo a eficácia e a segurança de potenciais terapias anti-metastáticas.
Um aspeto particularmente inovador do nosso ensaio é o uso de tecnologias de “organ-on-a-chip”. Estes chips microfabricados funcionam como moldes para culturas celulares (3), permitindo compartimentalizar diferentes tipos de células, neste caso células tumorais e endoteliais, e manter zonas de interação entre elas.
Para além disso, permitem isolar as células em três dimensões, formando vasos sanguíneos em microescala, com fluxo controlado, o que simula as condições reais de irrigação de um tumor.
Em suma, ao aplicar estas tecnologias avançadas, conseguimos recapitular de forma mais fiel, em laboratório, os eventos de intravasão tumoral.
Estes progressos refletem o dinamismo da investigação em curso e reforçam a importância de promover o conhecimento científico no combate ao Cancro da Mama Metastático.
Com esta plataforma, acreditamos poder acelerar a descoberta de novas estratégias preventivas ou terapêuticas para prevenir a metastização, contribuindo para salvar a vida de mais doentes com Cancro da Mama.
Agradecimentos: Narmada Perera, Diogo Coutinho, Carolina Morais, David Barata, William Roman, Edgar Gomes, Cláudio Franco, Luís Costa, Karine Serre, Sérgio Dias e equipa de bioimagem do GIMM.
Referências: 1. Siegel, R. L., Miller, K. D., Wagle, N. S. & Jemal, A. Cancer sta1s1cs, 2023. CA Cancer J Clin .2023. 2. Gerstberger S, Jiang Q, Ganesh K. Metastasis. Cell. 2023. 3. Bhatia, S., Ingber, D. Microfluidic organs-on-chips. Nat Biotechnol. 2014